Проблеме лечения посттравматической костной дисрегенерации посвящено значительное количество работ, в которых рассматриваются как хирургические, так и нехирургические методы стимуляции репаративного остеогенеза. Однако, несмотря на достаточно высокий процент успешного лечения больных с нарушением процессов консолидации костных отломков, у 4,8 – 15,4% больных достичь положительных результатов не удается. Наибольшие трудности при лечении нарушений остеорепарации возникают после травм, полученных в результате воздействия высокоэнергетического травмирующего агента. По данным разных источников у 10,8 – 13,7% больных с высокоэнергетическими травмами нижних конечностей переломы не срастались в течение 1,5 – 3 лет. Известно, что формирование костной мозоли в области перелома происходит благодаря клеткам-предшественникам периоста, эндоста и мезенхимальным стромальным (стволовым) клеткам костномозговой полости (МСК КП). Одним из определяющих механизмов формирования костной мозоли является остеогенная дифференцировка пролиферирующих в костную рану клеток-предшественников. Исследования последних лет показали, что дифференциация МСК по остеобластическому типу представляет собой сложный, многогранный процесс и осуществляется под контролем факторов транскрипции, клеточных и матриксных взаимодействий, системных и местных факторов. На процессы остеогенной дифференциации значительное воздействие оказывает большое количество местных факторов, подавляющее большинство которых продуцируется клетками остеобластической линии. Но, несмотря на то, что в процессе остеогенной дифференцировки мигрирующих в костную рану клеток-предшественников, ведущее значение играют паракринные факторы, продуцируемые уже имеющими остеогенную направленность клетками периоста и эндоста, работ, посвященных изучению изменений морфофункционального состояния клеточных источников остеорепарации в зависимости от механизма травмы и роли этих изменений в развитии дисрегенерации, в доступной литературе найти не удалось.
В связи с этим было проведено изучение роли изменений морфофункционального состояния клеточных источников остеорепарации (периоста, эндоста и мезенхимальных стромальных клеток костномозговой полости (МСК КП) в нарушении репаративного остеогенеза. Для этого были проведены экспериментальные и клинические исследования. Изучали морфологическую картину области костной раны и морфофункциональное состояние клеточных источников остеорепарации (периоста, эндоста и МСК КП).
Экспериментальные исследования проводились in vivo и in vitro на 80 половозрелых белых беспородных крысах самцах. Животных подразделили на три группы – контрольную, первую и вторую. Контрольную группу образовали десять животных. У этих животных при помощи МТТ-анализа изучали пролиферативную активность клеток периоста, эндоста и МСК КП. Для чего после выведения из эксперимента у интактных животных в асептических условиях осуществляли отчленение обеих голеней и выделение из мягких тканей берцовых костей. Берцовые кости помещали в специальный консервант и выдерживали в нем в течение суток. Затем в стерильных условиях ножницами отсекали метаэпифизарные области, оставляя для дальнейшего исследования только диафизарную часть кости. Для определения пролиферативной активности МСК КП в стерильных условиях из костномозгового канала при помощи инсулинового шприца и физиологического раствора вымывали костномозговое содержимое в чашки Петри с культуральной средой. Для упрощения этой процедуры диафизарную часть кости рассекали поперечно пополам. Половина костных фрагментов рассекалась продольно глазными ножницами, тщательно отмывали от остатков костномозгового содержимого физиологическим раствором и помещали в чашки Петри с коллагеновой подложкой и питательной средой таким образом, чтобы с коллагеновой подложкой контактировала только надкостница (рис. 1 а). Такое положение костных фрагментов в чашках Петри создавало условия для пролиферации только клеток надкостницы. Оставшуюся половину костных фрагментов при помощи скальпеля, тщательно очищали от надкостницы, промывали физиологическим раствором и помещали в чашки Петри с коллагеновой подложкой и питательной средой таким образом, чтобы с коллагеновой подложкой контактировала костная ткань (рис. 1 б). Это создавало условия для пролиферации только клеток собственно костной ткани (клеток эндоста).

Чашки Петри с костномозговым содержимым и костными фрагментами помещали в СО2-инкубатор и культивировали при стандартных условиях (температуре 37°С и 5% содержании СО2) ос сменой питательной среды каждые третьи сутки. После начала клеточной пролиферации в чашках Петри с костными фрагментами последние аккуратно извлекались, а прикрепившиеся к коллагеновой подложке клетки продолжали культивировать. МТТ-анализ пролиферативной активности клеток периоста, эндоста и МСК КП осуществляли на 14-е сутки культивирования. Полученные результаты были приняты как контрольные.
У животных первой (35 крыс) и второй (35 крыс) групп моделировали низко- и высокоэнергетические переломы берцовой кости. При моделировании низкоэнергетических травм (первая группа) в асептических условиях, под эфирным наркозом в области средней трети голени скальпелем осуществляли разрез кожи и выделяли берцовую кость. Узким долотом выполняли остеотомию кости в средней трети, после чего рану зашивали наглухо. При моделировании высокоэнергетических переломов (2 группа) под эфирным наркозом в области средней трети голени при помощи пружинного устройства наносили дозированный удар, сила которого составляла в среднем 2,55±0,04 кг×м/с. У 10 животных (по 5 животных каждой группы) травмированные сегменты фиксировали параоссально с использованием игл для внутримышечных инъекций и полихлорвиниловых трубок для внутривенных инфузий. Выведение этих животных из эксперимента осуществляли на 7 сутки после нанесения травмы. После выведения из эксперимента у животных в асептических условиях отчленяли травмированный сегмент, освобождали его от шкуры, фиксировали в 10%-растворе нейтрального формалина, декальцинировали и окрашивали гематоксилином и эозином. Полученные гистологические препараты изучали в световом микроскопе. Шестьдесят животных (по 30 животных каждой группы) были выведены из эксперимента через 1 час после нанесения травмы. После выведения из эксперимента у животных в асептических условиях отчленяли травмированный сегмент, костные фрагменты аккуратно выделяли из мягких тканей и помещали во флакон со стерильным консервантом. Костные фрагменты выдерживали во флаконе с консервантом в течение одних суток. Затем с костными фрагментами каждого из животных выполняли те же манипуляции, что и у животных контрольной группы и культивировали в СО2-инкубаторе при стандартных условиях. На 5 – 8-е сутки культивирования при помощи фазово-контрастной микроскопии осуществляли подсчет пролиферирующих от костных фрагментов клеток периоста и эндоста. Клетки подсчитывали в поле зрения микроскопа при 100-кратном увеличении на пяти уровнях от линии перелома. В качестве критерия, определяющего уровень подсчета, использовали поле зрения микроскопа. На 14-е сутки культивирования в 45-ти чашках Петри каждой группы (по 15 чашек для каждой из клеточных культур) методом МТТ-анализа определяли пролиферативную активность клеток периоста, эндоста и МСК КП. В остальных 45-ти чашках Петри каждой группы (по 15 чашек для каждой из клеточных культур), после формирования монослоя при помощи фазово-контрастной микроскопии оценивали морфологическое состояние пролиферирующих клеток надкостницы, эндоста и МСК КП. В монослое культур периоста и эндоста при помощи реакции с BCIP/NBT Liquid Substrate System (Sigma, США) определяли наличие или отсутствие продукции клетками щелочной фосфатазы (ЩФ), что позволяло судить о наличии или отсутствии остеогенной детерминированности (направленности) клеток.
Клинические исследования были проведены у 5-ти больных с длительным несрастанием переломов длинных костей нижних конечностей. У 2-х больных имелись несросшиеся переломы бедренной кости, у 3-х больных – большеберцовой кости. Продолжительность нарушения целостности костной ткани у этих больных была от 11 месяцев до 2 лет. Во время оперативном лечения у больных из проксимального костного фрагмента в области перелома осуществляли забор периостальных тканей размером 0,5´0,5 см. Биопсийный материал помещали во флакон с консервантом и выдерживали в течение суток. Затем в стерильных условиях участки периоста извлекали из консерванта и помещали в чашки Петри с питательной средой и культивировали в СО2-инкубаторе при стандартных условиях. После появления клеточной пролиферации периостальные ткани извлекались, а прикрепившиеся к пластику клетки культивировались до формирования монослоя. При помощи фазово-контрастной микроскопии оценивали морфологическое состояние пролиферирующих клеток периоста, а при помощи реакции на ЩФ – их остеогенную детерминированность.
Фотодокументирование клеточных культур и гистопрепаратов осуществляли с помощью инвертированного микроскопа Leica DMIL, рабочей станции по обработке изображений Leica QWin500 Standart (версия 2.3, сэр. № 3069) и видеокамеры Sanyo TK-C1380 (Германия). Полученный в результате исследований цифровой материал подвергали статистической обработке.
При изучении гистоморфологических препаратов области костной раны на 7-е сутки после травмы было отмечено, что состояние костных фрагментов и сращение переломов у животных первой и второй групп было различно. У животных первой группы костные фрагменты имели значительное количество клеточных элементов с хорошо прокрашенными ядрами. В области костной раны происходило образование примитивных костных балок, характерных для процессов формирования костной мозоли (рис. 2а). Во второй группе количество клеточных элементов в костной ткани отломков было во много раз меньше, чем в первой группе. Они располагались преимущественно в удаленных от линии перелома участках костной ткани. В кости, прилегающей непосредственно к линии перелома, встречались единичные клетки со слабо прокрашенными ядрами. Данные изменения морфологически напоминали картину остеонекроза. В области перелома репаративные процессы проявлялись в виде формирования грубоволокнистой ретикулярной соединительной ткани, заполняющей костную рану (см. рис. 2б).

Таким образом, данные гистоморфологических исследований свидетельствуют о том, что интенсивность воздействующего на кость травмирующего агента оказывает влияние состояниее костной ткани и течение сращения перелома. При низкоэнергетических травмах в костной ране репаративные процессы протекают с формированием специфического костного регенерата, а при высокоэнергетических травмах репаративные процессы ограничиваются образованием неспецифического рубцового регенерата.
При культивировании клеток надкостницы активная клеточная пролиферация начиналась на 5-6-е сутки. У животных первой группы клетки надкостницы пролиферировали равномерно вдоль всего костного фрагмента (рис 3а). У животных второй группы пролиферация клеток надкостницы вдоль костного фрагмента была неравномерной. В зоне, прилегающей к линии перелома, пролиферировали единичные клетки. Активная клеточная пролиферация отмечалась в зоне, наиболее удаленной от линии перелома (рис. 3б).

Результаты подсчета количества клеток периоста у животных 1 и 2 групп представлены в таблице 1 и на диаграмме (рис. 4).

Представленные данные свидетельствуют о том, что у животных первой группы количество пролиферирующих клеток было одинаково на всем протяжении костного фрагмента и составляло 27-29 клеток в поле зрения. Во второй группе животных количество пролиферирующих клеток в области перелома не превышало 6-ти в поле зрения. В более удаленных от линии перелома зонах количество пролиферирующих клеток постепенно увеличивалось с 17 до 54 клеток. Различия в количестве клеток между уровнями от линии перелома у животных второй группы имели достоверный характер (между 1, 2 и 3 уровнями – t=2,39, р < 0,05; между 3 и 4 уровнями – t=2,3, р < 0,05; между 4 и 5 уровнями – t=2,2, р < 0,05).
Сопоставление количества клеток на 1 – 5-м уровнях у животных двух групп показало, что у животных первой группы, на первых трёх уровнях количество пролиферирующих клеток значительно превышало таковое у животных второй группы (р < 0,002 и р < 0,05). На четвертом уровне количество пролиферирующих клеток надкостницы в обеих группах было примерно одинаковым (р > 0,10), а на пятом уровне от линии перелома различия имели обратную зависимость. В этой области количество пролиферирующих клеток во второй группе было достоверно большим, чем в первой группе (р < 0,05).
В процессе культивирования пролиферативная активность клеток периоста у животных двух групп была выше контрольного значения. Пролиферативная активность клеток периоста в первой группе была в 1,6 раза (t= 7,8; р < 0,001), а во второй в 1,4 раза (t= 7,7; р < 0,001) больше контрольных значений. Различия между пролиферативной активностью клеток периоста первой и второй групп также имели достоверные различия, хотя и были менее выражены (t= 2,2; р < 0,05) (табл. 2).

При формировании клеточного монослоя, отмечали наличие морфологических отличий между клетками надкостницы у крыс первой и второй групп. Во всех наблюдениях у животных первой группы клетки надкостницы имели веретенообразную форму, плотно прилегали одна к другой и располагались параллельно (рис. 5а). Во второй группе пролиферирующие клетки надкостницы имели звездчатую (отростчатую) форму с явно выраженными отростками цитоплазмы. Периостальные клетки животных второй группы, в отличие от периостальных клеток животных первой группы, в процессе культивирования образовывали субконфлуэнт, который имел «сетчатую» структуру (см. рис. 5б).
При выявлении продукции культивированными клетками периоста ЩФ положительную реакцию наблюдали только у животных первой группы (рис. 6). Периостальные клетки животных второй группы ЩФ не продуцировали.


Весьма показательно, что подобная картина наблюдаласт при исследовании периостальных тканей, полученных в ходе оперативного лечения пострадавших с нарешениями остеорепарации после переломов костей. Так, в процессе культивирования тканей периоста, взятых у больных во время оперативного лечения, наблюдали формирование монослоя, который образовывали гетерогенные клетки. В монослое наблюдали как продолговатые веретенообразные клетки, так и клетки округлой формы и больших размеров с цитоплазматическими выростами (рис. 7). По своей морфологической картине монослой, образованный этими клетками, напоминал монослой, образованный клетками животных второй группы. Постановка реакции с BCIP/NBT показала, что среди пролиферирующих клеток имеются единичные веретенообразные клетки, слабо продуцирующие ЩФ.

При изучении пролиферации клеток эндоста наблюдали картину, схожую с пролиферацией клеток периоста. Эндостальные клетки начинали пролиферировать на 7–8-е сутки культивирования. Количество пролиферирующих эндостальных клеток, как и в случае с клетками периоста, на разных уровнях от линии перелома в двух группах было различно (табл. 3, рис. 8).

У животных первой группы количество пролиферирующих клеток эндоста на всем протяжении костного фрагмента было примерно одинаковым и колебалось от 35 до 50 в поле зрения. У животных второй группе в области перелома количество клеток эндоста не превышало 12-13 в поле зрения, а в зонах удаленных от перелома увеличивалось в 3-4 раза и колебалось от 33 до 49 клеток. У животных этой группы достоверные различия в количестве пролиферирующих клеток отмечались только между 1-2 уровнями и 3 уровнем (t=2,7, р < 0,02). Различий между 3, 4 и 5 уровнями не было (t=0,4, р > 0,10; t=0,23, р > 0,10 соответственно). Сопоставление количества клеток на 1 – 5-м уровнях у животных двух групп показало наличие достоверных различий только на первых двух уровнях – t=4,24, р < 0,001 для первого уровня и t=2,74, р < 0,02 для второго уровня. Морфология клеток эндоста у животных первой и второй группы была неодинакова. У животных первой группы клетки имели округлую форму, характерную для остеобластных клеток (рис 9а). У животных второй группы пролиферирующие клетки напоминали фибробластоподобные клетки (рис 9б).

При культивировании эндостальных клеток животных двух групп было установлено, что пролиферативная активность клеток эндоста у животных двух групп имела достоверные отличия. У животных первой группы пролиферативная активность клеток эндоста практически не отличалась от контрольных значений (t= 2,7; р < 0,05). Пролиферативная активность эндостальных клеток животных второй группы была достоверно выше контрольных значений и пролиферативной активности клеток эндоста животных первой группы (t= 5,8; р < 0,001 и t= 5,4; р < 0,001 соответственно) (табл. 4).

К 14-м суткам культивирования эндостальные клетки животных первой группы формировали субконфлуэнтную структуру с остеобластоподобными клетками, активно продуцирующими ЩФ (рис. 10а). Эндостальные клетки животных второй группы к этому времени формировали плотный монослой, образованный фибробластоподобными клетками, не продуцирующими ЩФ (рис. 10б).

При фазово-контрастной микроскопии первичных культур мезенхимальных стромальных клеток, выделенных из костномозгового канала травмированных сегментов, было отмечено, что у животных первой группы количество МСК, адгезировавших к пластику, было примерно в 10-12 раз больше, чем у животных второй группы (рис. 11). Так как способностью адгезировать к пластику обладают только жизнеспособные МСК, то данные микроскопии первичных культур позволяют говорить о том, что в костномозговом канале под воздействием травмирующего агента высокой интенсивности происходит гибель значительного количества МСК.

По данным МТТ-анализа пролиферативная активность МСК на 14-е сутки культивирования у животных первой группы была в 3,5 раза выше контрольных значений (t= 9,9; р < 0,001), а у животных 2 группы – в 2,5 раза (t= 7,5; р < 0,001). Различия в пролиферативной активности МСК между группами имели достоверный характер – пролиферативная активность МСК животных первой группы была в 1,4 раза выше, чем у животных второй группы (t= 3,2; р < 0,01) (табл. 5).

К 14-м суткам культивирования МСК КП животных первой группы формировали плотный монослой с клетками округлой формы, которые по своей морфологии напоминали эпителоидные клетки (рис. 12а). МСК КП животных второй группы к этому времени формировали субконфлуэнт. По своей структуре субконфлуэнт, образованный этими клетками, напоминал субконфлуэнт, образованный клетками периоста животных этой же группы (см. рис. 5б) – одна часть клеток имела веретенообразную форму, а вторая часть – звездчатую (рис. 12б).

При сопоставлении пролиферативной активности различных клеточных источников остеорепарации у животных контрольной, первой и второй групп было отмечено, что клетки периоста и МСК, как в контрольной, так и в первой и второй группах, обладают большей пролиферативной активностью, чем клетки эндоста. У животных контрольной группы различий между пролиферативной активностью периостальных клеток и МСК не отмечалось (t = 0,63; р > 0,10), а по отношению к пролиферативной активности эндостальных клеток эти различия носили достоверный характер (t = 24,01; р < 0,001 и t = 27,69; р < 0,001 соответственно) (табл. 6, рис. 13).

Данное различие обусловлено тем, что клетки периоста и МСК являются менее дифференцированными, чем клетки эндоста, которые, по своей сути, являются остеобластическими клетками, находящимися на разной стадии дифференцировки – от преостеобластов до остеобластов.
После нанесения травмы пролиферативная активность клеток из различных источников остеорепарации возрастала. Наибольшая активация процессов пролиферации отмечалась со стороны МСК костно-мозгового канала. У животных первой группы пролиферативная активность МСК КП была в 2,2 раза выше, чем клеток периоста (t = 7,2; р < 0,001) и в 11,3 раза больше чем клеток эндоста (t = 12,55; р < 0,001). У животных второй группы пролиферативная активность МСК КП была больше пролиферативной активности клеток периоста в 1,8 раза (t = 5,37; р < 0,001) и в 4,3 раза больше, чем у клеток эндоста (t = 9,49; р < 0,001). На втором месте по пролиферативной активности находились клетки периоста. В первой группе их активность была в 5,2 раза выше, чем активность эндостальных клеток (t = 16,1; р < 0,001), а во второй группе – в 2,4 раза больше (t = 12,7; р < 0,001). В тоже время пролиферативная активность клеток периоста и МСК КП у животных первой группы была достоверно выше, чем у животных второй группы (t = 2,19; р < 0,05 и t = 3,19; р < 0,01 соответственно). Со стороны клеток эндоста, наоборот, более выраженная пролиферативная активность отмечалась у животных второй группы (t = 5,35; р < 0,001).
Полученные в результате исследований данные свидетельствуют о том, что на течение репаративных процессов в костной ране значительное влияние оказывает характер травмы, а именно, интенсивность, с которой травмирующий агент воздействует на костную ткань. При травмах низкой интенсивности репаративные процессы, развивающиеся в костной ране, приводят к образованию костного регенерата и сращению перелома. При травмах высокой интенсивности в костной ране также протекают репаративные процессы, но они завершаются формированием неспецифической фиброзной ткани (см. рис. 2). Закономерно возникает вопрос: «Почему после воздействия травмирующего агента высокой интенсивности в области перелома не происходит формирования костного регенерата?». По нашему мнению, ответ на этот вопрос дают результаты проведенных исследований.
Полученные при исследованиях в условиях in vitro данные свидетельствуют о том, что при травмах высокой интенсивности клетки периоста, эндоста и МСК КП претерпевают определенные морфофункциональные изменения. Во-первых, при травме высокой интенсивности в костных фрагментах происходит гибель значительного количества клеточных элементов периоста и эндоста на значительном удалении от линии перелома. Количество способных к пролиферации клеток периоста в этой области сокращается более чем в 5 раз, а количество клеток эндоста уменьшается более чем в 3,5 раза. Большая часть МСК костномозгового канала также теряет свою жизнеспособность. В пользу этого говорит уменьшение более чем в 10 раз количества жизнеспособных МСК. Во-вторых, пролиферативная активность клеток периоста и МСК при травмах высокой интенсивности в 1,2 и 1,4 раза ниже, чем при травмах низкой интенсивности, а пролиферативная активность эндостальных клеток, наоборот, при травмах высокой интенсивности почти в 2 раза выше, чем при травмах низкой интенсивности. Последнее может быть объяснено дедифференцировкой эндостальных клеток, которая происходит в результате воздействия на костную ткань травмирующего агента высокой интенсивности. В пользу дедифференцировки клеток эндоста говорит изменение формы клеток – от округлой, характерной для остеобластных клеток, до веретенообразной, характерной для фибробластоподобных клеток, которые обладают большей пролиферативной активностью. В-третьих, при травмах высокой интенсивности клетки периоста и МСК КП теряют способность формировать монослой. Вместо монослоев, образованных упорядоченными, имеющими одинаковую форму клетками, происходит формирование субконфлуэнтных культур, образованных морфологически гетерогенными (в т.ч. гипертрофированными и некротизирующимися) клетками, которые имеют нехарактерную для клеток периоста и МСК форму (см. рис.5, рис. 7 и рис. 12). Клетки эндоста, в отличие от клеток периоста и МСК, формируют плотный монослой, но в образовании монослоя принимают участие клетки, имеющие фибробластоподобную, не характерную для клеток эндоста, форму (см. рис. 10). Кроме того, в результате воздействия травмирующего агента высокой интенсивности, периостальные и эндостальные клетки прекращают продуцировать ЩФ.
Также важно отметить, что клеточные культуры, полученные от группы животных с низкоэнергетической травмой, морфологически отличны от таковых, полученных от животных с высокоэнергетической травмой. Первые имеют эпителоидную морфологию (кроме клеток периоста) и являются остеобластными линиями (см. рис. 9а, 10а, 12а). Клетки периоста и эндоста животных первой группы активно продуцируют ЩФ, что свидетельствует об их остеогенной направленности и способности оказывать остеогенную индукцию малодифференцированных клеток костного мозга. В то же время, фибробластоидные клетки животных второй группы (см. рис. 9б, 10б, 12б) теряют свою остеогенную детерминированность (о чем свидетельствует отсутствие у них продукции ЩФ) и способность оказывать остеогенную индукцию малодифференцированных клеток костного мозга.
В работах последних лет было показано, что в костной ране под действием значительного количества биологически активных веществ происходит активация и миграция в костную рану пролиферирующих некоммитированных малодифференцированных МСК КП, по-сути являющихся прото-миофибробластами. При этом в участке перелома локально выделяется значительное количество ТФР-β, накапливается значительное количество специфического белка фибронектина, и возникают мощные силы натяжения экстрацеллюлярного матрикса, отражающие механические свойства матрикса и ремоделирующей активности клеток. Механорецепция между миофибробластами, приводит к значительной контракции образующейся в ране грануляционной ткани. После этого постепенно происходит реорганизация грануляционной ткани с запуском процесса апоптоза в миофибробластах и заселением на их место детерминированных и индуцированных клеточных элементов.
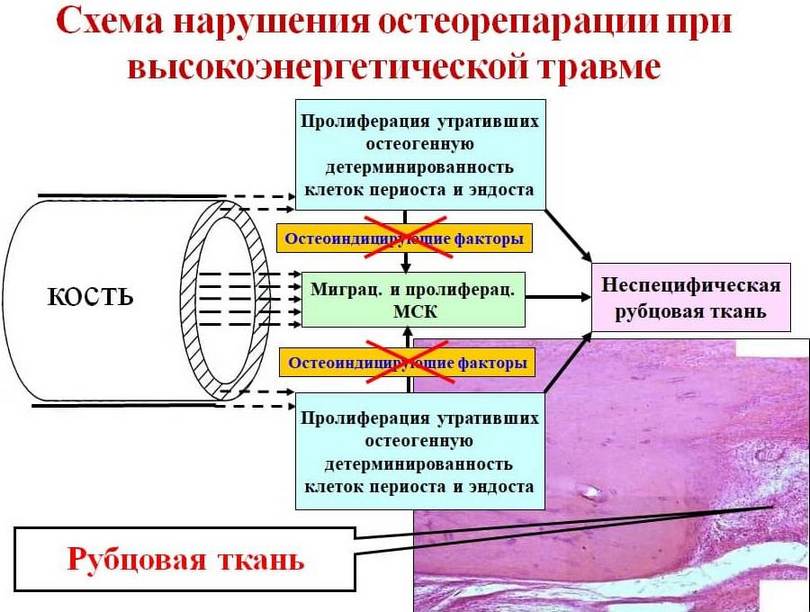
При переломах на место миофибробластов, подвергшихся апоптозу, приходят МСК из костномозгового канала и остеогенно детерминированные элементы эндоста и периоста. Перистальные и эндостальные клетки, наряду с формированием костного регенерата по периферии, остеоиндуцируют МСК, проникающие в грануляционную ткань, тем самым создавая условия для образования специфического костного регенерата во всей толще костной раны (рис. 12). В тех случаях, когда, в силу каких либо причин (в нашем случае в результате воздействия травмы высокой интенсивности), клетки периоста и эндоста теряют свою остеогенную детерминацию, остеоиндуцирующего воздействия с их стороны на МСК, находящиеся в грануляционной ткани, не происходит. В результате этого при реорганизации грануляционной ткани костной раны на место миофибробластов, подвергшихся апоптозу, из костномозгового канала, гаверсовых каналов и области периоста мигрируют морфологически измененные и утратившие присущие им остеогенные свойства фибробластоподобные клетки, которые способствуют образованию грубоволкнистого неспецифического рубца в месте перелома (рис 13).


Таким образом, обобщая все выше сказанное, можно говорить о том, что одной из основных причин, нарушающих течение репаративного остеогенеза, при травмах высокой интенсивности являются морфофункциональные изменения клеточных источников остеорепарации. Последние характеризуются дедифференцировкой остеогенно детерминированных клеток периоста и эндоста, что приводит к развитию остеогенной недостаточности, которая была описана В.Г. Гололобовым с соавт. на основании эмпирических заключений и подтверждена нашими экспериментальными исследованиями. Механизмы, приводящие к морфофункциональным изменениям клеточных источников остеорепарации, нам не известны и требуют отдельного изучения.